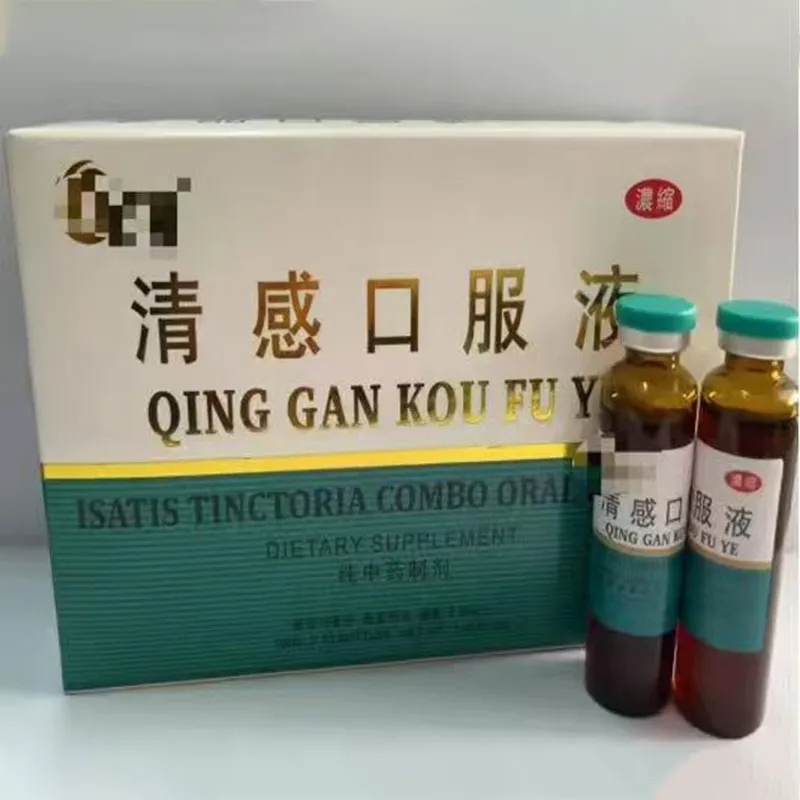
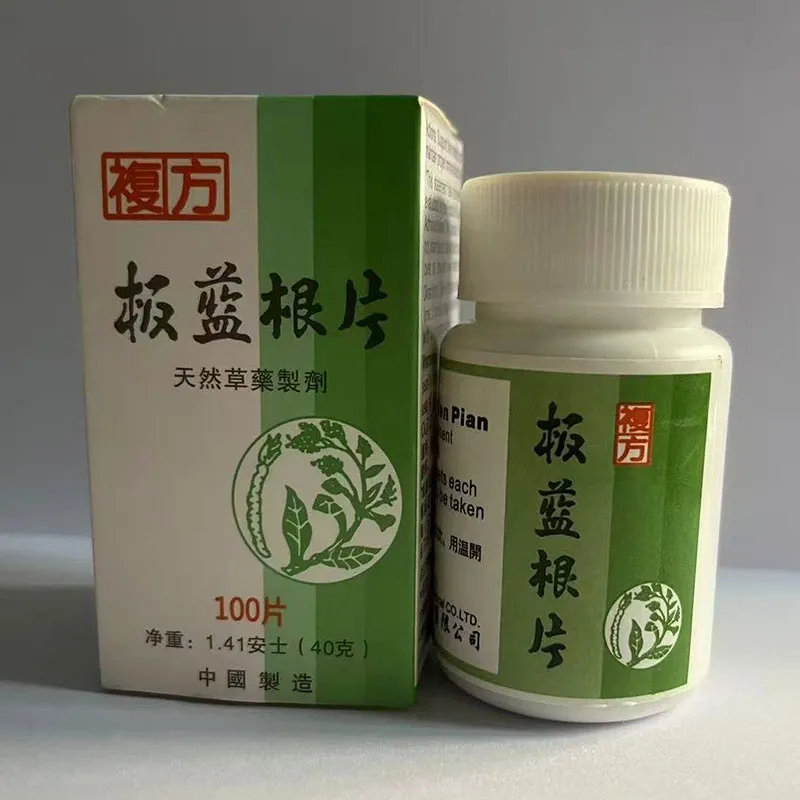
Фармацевтические пластиковые изделия производители
Когда слышишь 'производители фармацевтических пластиковых изделий', многие представляют просто литьё бутылочек. На деле же это адская комбинация химической стойкости, миграционной стабильности и бюрократии — тот редкий случай, когда технолог и юрист работают в обнимку. Сейчас объясню на примерах, почему даже GMP-сертификация не гарантирует, что партия не отправится в утиль из-за кривой горловины флакона.
Сырьё: где кроются неочевидные риски
Возьмём полипропилен для флаконов под сиропы — казалось бы, всё просто. Но если поставщик сменил катализатор на этапе синтеза гранул, а мы не провели миграционные испытания... Получаем историю 2018 года: крышки на партии 50 тыс. флаконов потрескались при стерилизации. Пришлось закупать немецкий стабилизатор, хотя изначально экономили на местном.
Особенно критично с первичными полимерами — некоторые китайские производители идут на хитрости, подмешивая регранулят. Для упаковки таблеток это может пройти, а вот для растворов для инъекций — катастрофа. Как-то раз на линии розлива заметили помутнение в зоне шва ампул. Оказалось, примеси в ПЭТГ дали реакцию с действующим веществом.
Сейчас работаем преимущественно с Sabic и Dow, но постоянно мониторим новых поставщиков. Вот недавно корейцы предложили биосовместимый поликарбонат — вроде бы всё сходится, но стоимость термостабилизатора съедает всю выгоду. Решили пока тестировать на пробных партиях крышек для капельниц.
Технологические ловушки: от допусков до смены инструмента
Литьё под давлением — это не про 'нажал кнопку и получил изделие'. Для флаконов под гранулы допустимое отклонение толщины стенки ±0,1 мм, но если пресс-форма изношена хотя бы на 5 микрон — уже брак. Как-то на производстве фармацевтической упаковки в Подмосковье запустили партию флаконов для антибиотиков, а потом выяснилось, что 30% не проходят контроль герметичности из-за микротрещин в зоне литника.
Особенно сложно с многослойным литьём — например, для чувствительных к кислороду препаратов. В 2021 году пытались воспроизвести технологию co-extrusion для флаконов с барьерным слоем EVOH. Полгода экспериментов, а стабильность параметров так и не добились — то деградация полимера, то расслоение в зоне шва. Пришлось вернуться к классическим решениям с поглотителями кислорода.
Сейчас рассматриваем вариант с японскими пресс-формами, но их стоимость — это 40% от всей линии. Может, стоит модернизировать существующие? Коллеги из ООО Аньхой Дуншэн Юбан Фармасьютикал (кстати, их сайт https://www.dsybzy.ru стоит изучить) показывали интересные решения по доработке литьевых машин — у них пять GMP-сертифицированных линий, включая линии для сиропов и капсул.
Контроль качества: почему визуального осмотра недостаточно
Многие до сих пор считают, что главное — отсутствие видимых дефектов. На самом деле основные проблемы начинаются на молекулярном уровне. Миграция пластификаторов — тихий убийца стабильности препарата. Помню, для одного заказчика делали ПВХ-плёнку для блистерной упаковки — вроде всё по регламенту, а через полгода хранения таблетки начали менять цвет.
Сейчас внедряем ВЭЖХ для скрининга миграции — дорого, но дешевле, чем отзыв партии. Кстати, у ООО Аньхой Дуншэн Юбан Фармасьютикал площадь зоны контроля качества — целых 1000 м2, что для производителя их масштаба довольно серьёзно. У нас же пока обходимся 400 м2, но планируем расширяться.
Самое сложное — это валидация методов очистки при смене продукта. Для линий капельниц иногда приходится делать до 15 промывок — и каждый раз отбирать смывы. Как-то раз недосмотрели за температурой моющего раствора — остатки полимера в труднодоступных местах спекались, потом три недели разбирали оборудование.
Регламенты и документация: бюрократия как необходимость
GMP — это не просто бумажка, а ежедневная работа с тысячами параметров. Особенно сложно с валидацией процессов — например, для литья крышек под паровую стерилизацию нужно документировать каждый градус в печи. Один раз чуть не провалили аудит из-за расхождения в 0,3°C между датчиками — пришлось менять всю систему термоконтроля.
Интересно, что у китайских коллег из ООО Аньхой Дуншэн Юбан Фармасьютикал GMP-сертификация с 2005 года, при этом они успешно прошли повторные проверки в 2010 и 2016 — значит, смогли выстроить систему не для галочки. У них 58 регистрационных удостоверений — серьёзный объём работы по согласованиям.
Сейчас готовим документы для регистрации новых флаконов под оральные растворы — уже полгода собираем данные по миграции, стерилизуемости, старению. Регуляторы с каждым годом ужесточают требования — в прошлом месяце вернули документы с требованием добавить испытания на устойчивость к УФ-излучению.
Логистика и хранение: нюансы, о которых не пишут в учебниках
Казалось бы, складирование готовой продукции — что может быть проще? Но для фармацевтического пластика критичны перепады влажности. Как-то приняли партию ПЭТ-преформ, а через месяц обнаружили, что 20% не поддаются выдуву — влага в материале вызвала гидролитическую деградацию. Теперь держим в цеху три осушителя.
Складские площади — отдельная головная боль. У того же ООО Аньхой Дуншэн Юбан Фармасьютикал под склады отведено 5000 м2 — это позволяет работать с большими партиями. Мы пока обходимся 2000 м2, но уже чувствуем ограничения — приходится чаще организовывать отгрузки, что увеличивает риски при транспортировке.
Особенно сложно с термочувствительными изделиями — например, поликарбонатные ёмкости для диагностических наборов. Летом пришлось заказывать рефрижераторы для доставки, хотя изначально в калькуляции этого не было. Клиент, конечно, недоволен повышением цены, но альтернативы нет.
Перспективы и тупиковые ветки развития
Сейчас все говорят про биоразлагаемые полимеры, но для фармацевтики это пока тупик. Испытывали PLA для упаковки травяных сборов — через два месяца хранения прочность снижалась на 40%. Может, стоит посмотреть в сторону перерабатываемых полиолефинов? Коллеги из Германии показывали интересные разработки по мономатериальной упаковке.
Ещё одно направление — умная упаковка с индикаторами качества. Пытались внедрить термохромные чернила для крышек — оказалось, они мигрируют в продукт. Теперь рассматриваем варианты с внешними индикаторами, но это удорожает логистику.
Если говорить о реалиях, то главный тренд — не инновации, а стабильность. Как показывает практика производителей фармацевтических пластиковых изделий, включая того же ООО Аньхой Дуншэн Юбан Фармасьютикал с их 221 сотрудником и 20-тысячной площадью, успех определяется не прорывными технологиями, а способностью годами поддерживать одинаковые параметры. Может, поэтому они смогли продержаться на рынке с 2005 года, пройдя три GMP-сертификации.
Соответствующая продукция
Соответствующая продукция
Самые продаваемые продукты
Самые продаваемые продукты-
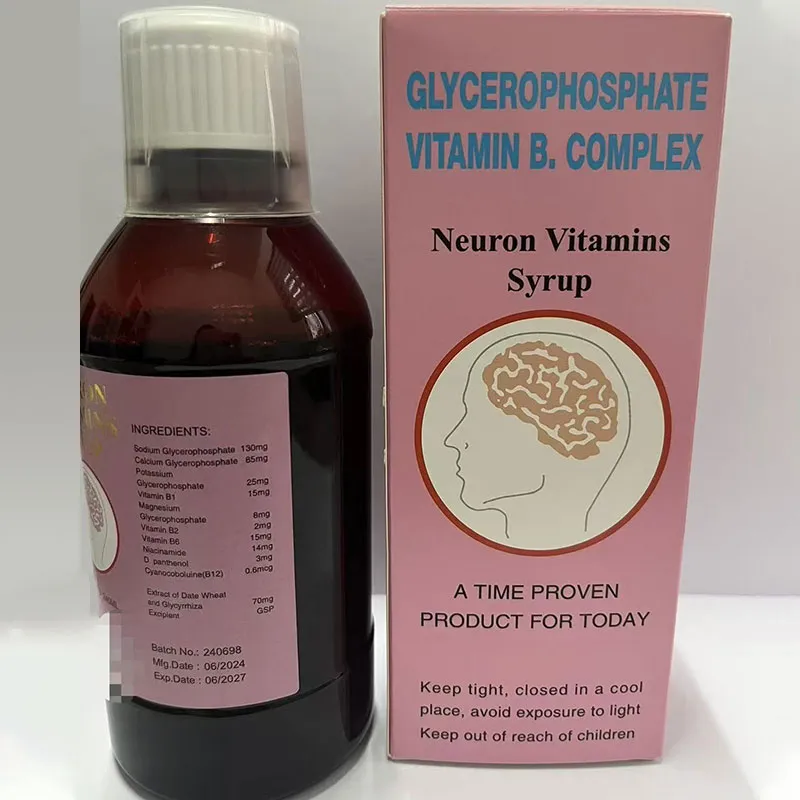 Успокаивающий витаминный сироп
Успокаивающий витаминный сироп -
 Капсулы для питания крови и роста волос
Капсулы для питания крови и роста волос -
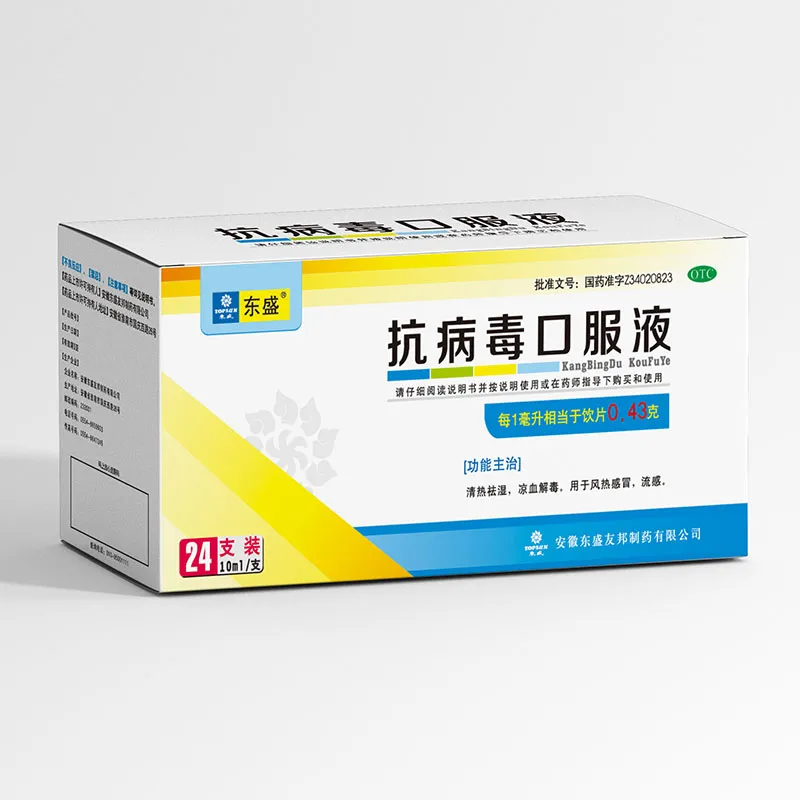 Противовирусный оральный раствор
Противовирусный оральный раствор -
 Экстракт пустырника
Экстракт пустырника -
 Таблетки с фаллопией многолетней для тонизации организма
Таблетки с фаллопией многолетней для тонизации организма -
 Таблетки с пачули для нормализации пищеварения при простуде
Таблетки с пачули для нормализации пищеварения при простуде -
 Чая для устранения сырости и очищения от жара
Чая для устранения сырости и очищения от жара -
 Таблетки коптис китайский для очищения жара
Таблетки коптис китайский для очищения жара -
 Таблетки ибупрофена
Таблетки ибупрофена -
 Гранулы «Полуденный чай» от простуды и для улучшения пищеварения
Гранулы «Полуденный чай» от простуды и для улучшения пищеварения -
 Раствор мемантина гидрохлорида для приема внутрь
Раствор мемантина гидрохлорида для приема внутрь -
 Гранулы Радикса Исатидис
Гранулы Радикса Исатидис
Связанный поиск
Связанный поиск- Уцзы яньцзун вань основный покупатель
- Уцзы яньцзун вань поставщики
- Капсулы гэнняньань для рассасывания уплотнений и устранения узлов в климактерический период производители
- Минму дихуан вань завод
- Стеклянный флакон для лекарств завод
- Улин вань производитель
- Цзяньпи вань завод
- Комплексные таблетки с лимонником китайским
- Гуйчжи фулин вань производители
- Цзинь гуй шэнь ци вань