
Нэй сяо ло ли вань завод
Когда слышишь 'Нэй сяо ло ли вань завод', многие сразу представляют стандартный китайский фармацевтический цех. Но на практике это сложный комплекс, где каждая деталь влияет на качество. Я работал с ООО Аньхой Дуншэн Юбан Фармасьютикал с 2012 года, и именно их подход к GMP показал, насколько важен не просто сертификат, а реальное соблюдение стандартов на каждом этапе.
GMP как основа, а не формальность
В 2005 году ООО Аньхой Дуншэн Юбан Фармасьютикал прошла полную сертификацию GMP. Но важно не это, а то, как они ее поддерживают. Например, в 2010-м была повторная сертификация, а в 2016-м — очередная. Я видел, как их команда готовилась: не для галочки, а с пониманием, что каждая проверка — это шанс улучшить процессы.
Особенно запомнилась их система контроля качества. Зона в 1000 м2 — это не просто площадь, а продуманная логистика. Пробы идут по четкому маршруту, исключающему перекрестное загрязнение. Мы как-то обсуждали, почему они не экономят на пространстве — оказалось, что для жидких форм (пероральные растворы, сиропы) это критично.
Их 58 регистрационных удостоверений — это результат не удачи, а системы. Каждый новый продукт тестируется с учетом особенностей линии. Например, для таблеток и гранул используются разные протоколы, хотя многие производители пытаются унифицировать процессы.
Персонал: цифры и реальность
221 сотрудник, из них 47 с профессиональным образованием. Цифра кажется скромной, но на деле эти 20% — костяк. Я общался с их технологами: они не просто имеют дипломы, а постоянно обучаются. Например, в 2018-м они внедрили новую систему контроля для капсул — инициатива исходила от рядовых инженеров.
Часто говорят, что в Китае кадры — слабое место. Но здесь я видел иное: специалисты знают свои зоны ответственности. Складские работники, например, понимают требования к хранению сиропов (температура, влажность), а не просто перемещают коробки.
Инфраструктура — отдельная тема. Их системы водоснабжения и электроснабжения не просто 'есть', а дублированы. Как-то раз во время визита случилась авария на линии пароснабжения — они переключились на резервную систему за минуты, без остановки производства. Это то, что не покажут в отчетах, но видно только при личном присутствии.
Площади: как они влияют на качество
20 000 м2 застройки — звучит масштабно, но ключ в распределении. Складские помещения 5000 м2 организованы с учетом сезонности. Например, для термочувствительных сиропов выделены зоны с климат-контролем, а не просто стеллажи.
Озелененная территория 4000 м2 — многим кажется излишеством. Но я видел, как это снижает пылевую нагрузку на производственные зоны. Особенно важно для линий таблеток и гранул, где чистота воздуха напрямую влияет на стабильность формул.
Зона контроля качества (1000 м2) — здесь нет мелочей. Помню, как они отказались от упрощенного теста для одной из партий капсул, обнаружив отклонение в скорости растворения. Решили переработать всю партию, хотя это ударило по срокам. Для меня это показатель зрелости производства.
Проблемы и решения: из практики
В 2015-м у них были сложности с масштабированием линии пероральных растворов. Оборудование не справлялось с возросшими объемами. Вместо покупки нового, они модернизировали существующее — пересмотрели параметры стерилизации, что дало прирост производительности на 15%.
Еще случай: при запуске нового сиропа столкнулись с нестабильностью вязкости. Оказалось, проблема в качестве сырья — поставщик изменил параметры без уведомления. Пришлось ужесточить входной контроль, добавив тесты на каждой партии. Теперь это стандарт для всех жидких форм.
С таблетками тоже не всегда гладко. Как-то раз партия не прошла тест на распадаемость — выяснилось, что влажность в цехе превысила норму. Решили установить дополнительные датчики, хотя изначально считали это избыточным. Теперь мониторят в режиме реального времени.
Перспективы и выводы
Статус провинциального частного научно-технического предприятия (с 2005 года) — это не просто табличка. Они реально инвестируют в R&D. Например, сейчас тестируют новую форму гранул с улучшенной биодоступностью — я видел прототипы на их сайте dsybzy.ru.
Что касается Нэй сяо ло ли вань завод — для меня это пример того, как можно сочетать масштаб и качество. Их сила не в размерах, а в деталях: от дублированных систем энергоснабжения до продуманной логистики складов.
Если резюмировать: работа с ними научила меня, что GMP — это не документ, а культура. И их повторные сертификации (2010, 2016) это подтверждают. Да, есть нюансы, но в целом — это производство, где понимают суть фармацевтики, а не просто гонятся за объемами.
Соответствующая продукция
Соответствующая продукция
Самые продаваемые продукты
Самые продаваемые продукты-
 Таблетки комплексного состава с шалфеем для улучшения кровообращения
Таблетки комплексного состава с шалфеем для улучшения кровообращения -
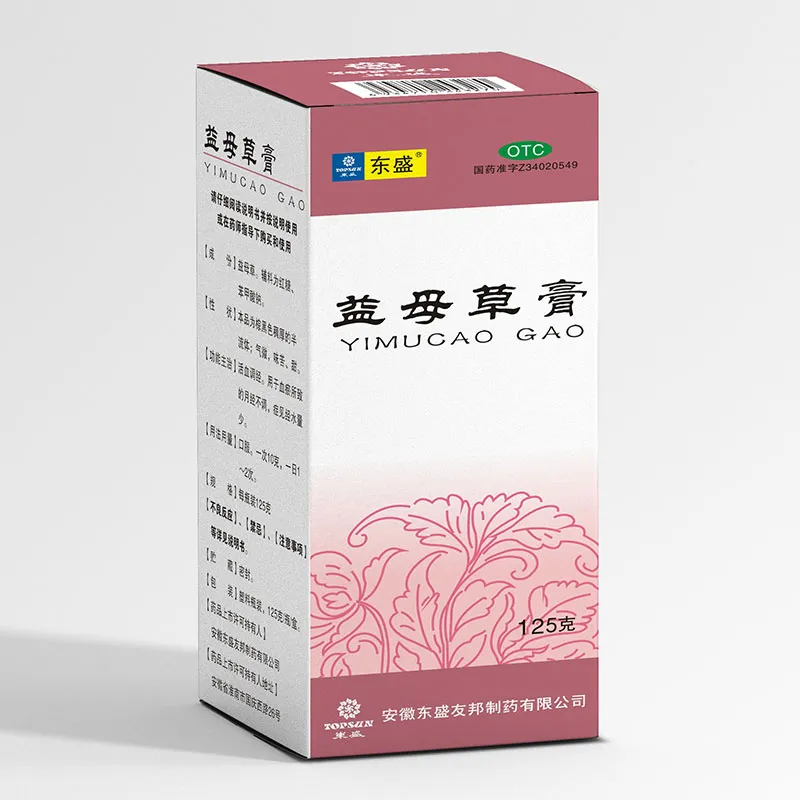 Экстракт пустырника
Экстракт пустырника -
 Чая для устранения сырости и очищения от жара
Чая для устранения сырости и очищения от жара -
 Таблетки коптис китайский для очищения жара
Таблетки коптис китайский для очищения жара -
 Седативно-ноотропный сироп
Седативно-ноотропный сироп -
 Сироп для укрепления печени
Сироп для укрепления печени -
 Капсулы для питания крови и роста волос
Капсулы для питания крови и роста волос -
 Поливитаминный питательный сироп
Поливитаминный питательный сироп -
 Капсулы с парацетамолом, кофеином, искусственным бычьим желчом и хлорфенамином
Капсулы с парацетамолом, кофеином, искусственным бычьим желчом и хлорфенамином -
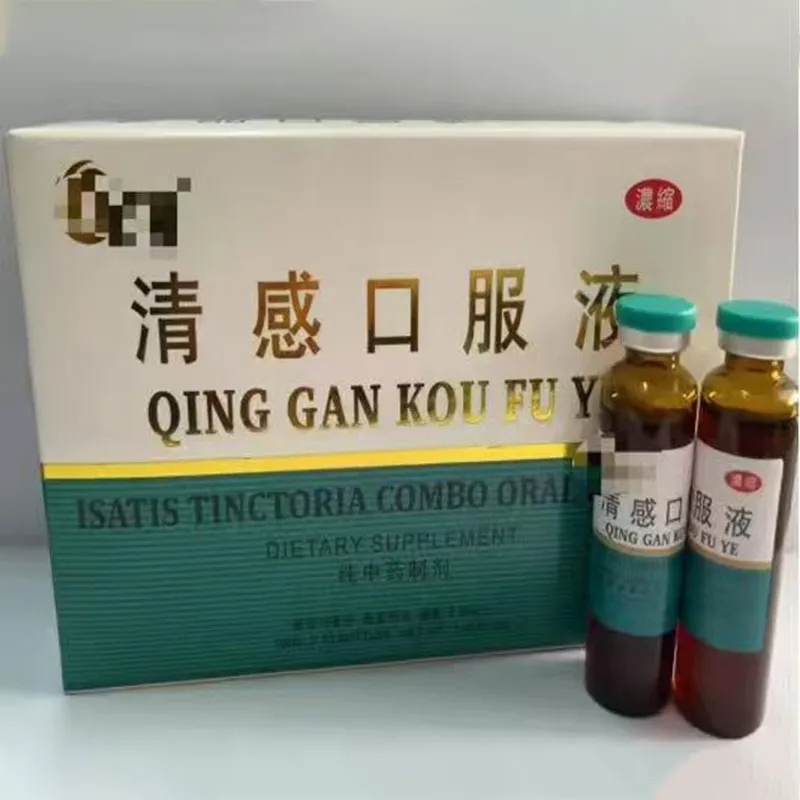 Раствор для приема внутрь «Снятие симптомов и очищение от жара»
Раствор для приема внутрь «Снятие симптомов и очищение от жара» -
 Таблетки от симптомов простуды и гриппа
Таблетки от симптомов простуды и гриппа -
 Гранулы «Полуденный чай» от простуды и для улучшения пищеварения
Гранулы «Полуденный чай» от простуды и для улучшения пищеварения
Связанный поиск
Связанный поиск- Очищающие жар выводящие токсины и устраняющие огонь гранулы цинцзе цзеду для снижения жара и детоксикации
- Раствор из желчи змеи и корня фритиллярии для отхаркивания и устранения кашля поставщик
- Желатиновые капсулы завод
- Защита и укрепление печени производители
- Флакон 10 мл стеклянный с крышкой заводы
- Шицюань дабу вань производитель
- Очищающие жар выводящие токсины и устраняющие огонь раствор цингань для облегчения симптомов простуды завод
- Баохэ вань поставщик
- Сянша янвэй вань цена
- Цяньлешу вань цена








